PKH26 Red Fluorescent Cell Linker Kit
储存条件:避光冷藏,如有结晶需在37℃水浴溶晶。因在乙醇中贮藏,所以要盖紧防挥发。稀释液C:常温或冰箱保存,保持无菌。
亲脂性染料结合到细胞膜上完成标记。染色强度是染料浓度和细胞浓度的函数,与渗透性无关。因此,保证染料添加量不过量非常关键。过标记的细胞将会导致细胞膜完整性缺失和或降低细胞活性。
下列过程可用于体内体外细胞的标记,包括干细胞、淋巴细胞、单核细胞、内皮细胞、神经细胞或者任何其他细胞。体内细胞的标记过程需一定的改进,如血小板的染色,或者选择性标记吞噬细胞。
无菌操作示范步骤(总体积2ml,染色终浓度为2×10-6M PKH26染料和1×107细胞/ml,所有操作在20~25℃)
2. 400×g离心5分钟形成松散的细胞团。注意:PKH26染料不能直接加到离心沉淀中,这样会造成细胞染色不均一和细胞活力降低。
3. 离心后,小心吸弃上层清液,细胞团上剩余液体<25ul。注意:为得到可重复的实验结果,在用稀释液C重悬时,减少残留培养基或缓冲液体积。
4. 加入1mL稀释液C,用移液管轻轻吹打混匀,制备2×细胞悬液。重悬细胞保证完全离散,别震荡,不要让细胞在稀释液C中保存太长时间。
注意:生理盐的存在会使得染料结团并大幅降低染色效率。需确保染色时细胞悬浮于稀释液C中,不含培养基或缓冲盐。
5. 临染色之前,将4μL PKH26乙醇溶液加入1mL稀释液C中,充分混匀,配制的2×染色液(4×10-6M)。
注意1:为减少乙醇对细胞活率的影响,步骤5加入的染料使得步骤6中乙醇最终浓度不能超过1-2%。
注意2:如果所需染料最终浓度<2×10-6M,需用100%乙醇将PKH26稀释于另一单独的容器中,以确保实验结果的可重复性。
注意:由于染色瞬间完成,快速将细胞与染料混匀对得到明亮、均匀和可重复的标记结果非常重要。为获得最佳效果应采取下述措施:
b. 将2×细胞悬液(步骤4)与2×染色液(步骤5)等体积混合。
c. 调整2×细胞和2×染料的浓度避免染色体积太小(<100μL)或太大(>5mL)。
d. 用电动移液器快速将细胞和染料混匀。血清移液管混匀速度太慢而使得染色不均匀。震荡和旋涡震荡混匀同样混匀较慢,染色均一性差。
e. 分配体积尽量准确,以保证样品与样品之间,实验与实验之间的可重复性。
7. 混匀后的染色的细胞25℃孵育的2-5min,定时轻轻颠倒离心管保证在25℃充分混匀。由于染色速度较快,延长孵育时间对实验没有帮助。
8. 加入等体积的血清(2mL)或加入等量血清或1%BSA中止染色反应,孵育1min以结合多余的染料。
注意1:血清(或等效的蛋白浓度)为最优的终止液。如果用完全培养基(含血清的组织培养基)替代,添加体积为10mL。
注意3:不要用无血清培养基或缓冲盐,他们会使染料产生聚集。染料聚集使清洗过程中无法洗净,使得分析过程中仍存在未标记的细胞。
注意1:将重悬液转移至新离心管中,减少了离心管壁残留的染料对洗涤效率的影响;注意2:不要用稀释液C清洗。
10. 最后一步清洗后,用10mL完全培养基重悬细胞评估细胞回收率,细胞活率和荧光强度。离心重悬细胞至所需活细胞浓度。
注意1:染色后的细胞可以用中性甲醛固定,避光条件下,荧光强度至少3周内保持稳定。
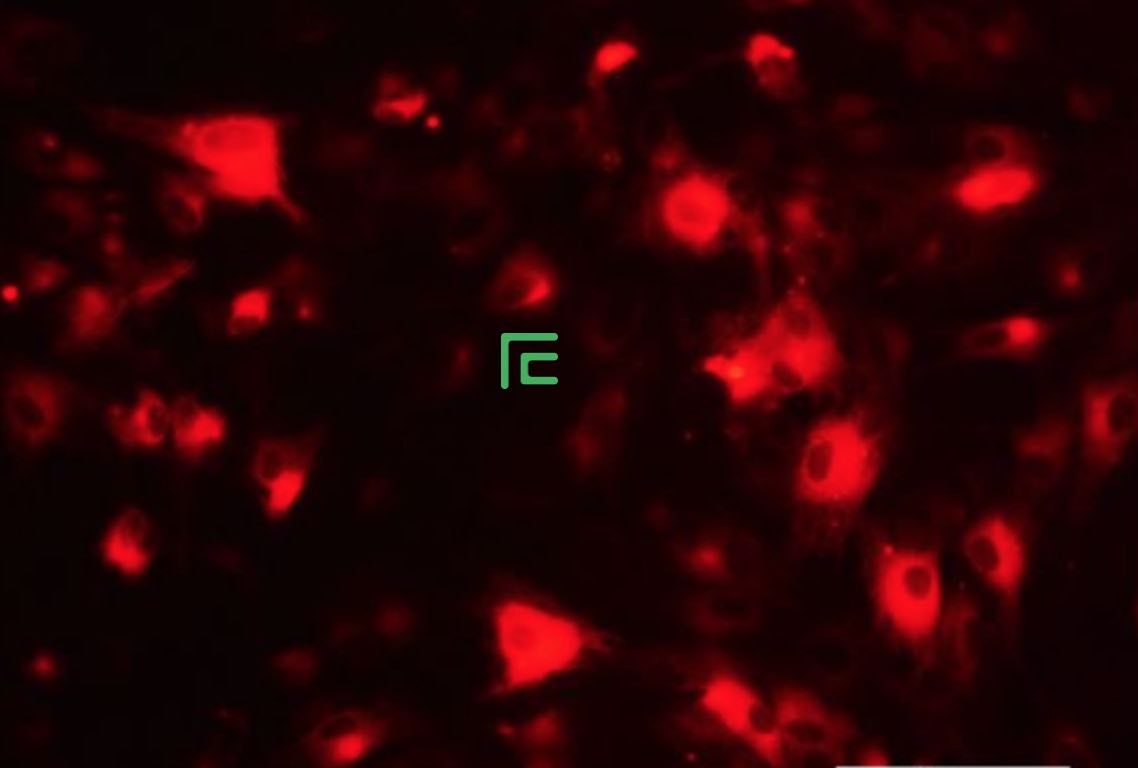
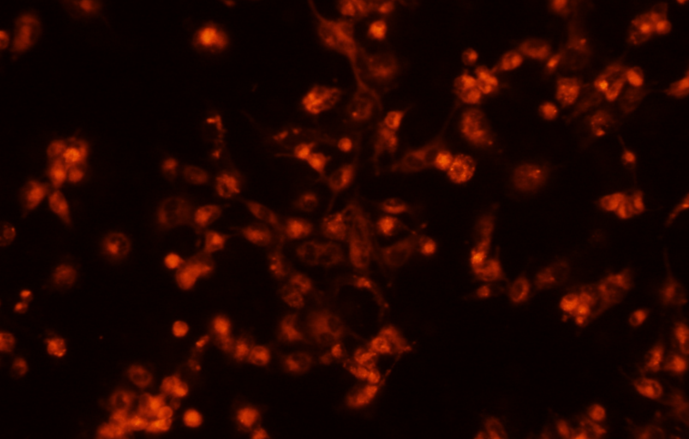
注意2:染色荧光强度一般为背景的100-1000倍。虽然染色的CV值与细胞种类有关,但荧光分布应该尽量均匀对称。
11. 荧光显微镜/流式细胞仪分析细胞。检查细胞复苏情况、传代情况及荧光浓度。染色应均匀,比本底荧光高100-1000倍。
| Name | PKH26红色荧光细胞链接试剂盒 PKH26 Red Fluorescent Cell Linker Kit | ||
|---|---|---|---|
| CAT# | PKH26 | CAS# | 154214-55-8 |
| Storage# | 4°C Sealed & desiccated & Minimized light exposure | Shelf Life# | 24 months |
| Ex(nm)# | Em(nm)# | ||
| MW# | Solvent# | ||
| Name | PKH26红色荧光细胞链接试剂盒 PKH26 Red Fluorescent Cell Linker Kit |
|---|---|
| CAT# | PKH26 |
| CAS# | 154214-55-8 |
| Storage# | 4°C Sealed & desiccated & Minimized light exposure |
| Shelf Life# | 24 months |
| Ex(nm)# | |
| Em(nm)# | |
| MW# | |
| Solvent# |
 详细说明书
详细说明书 技术资料
技术资料