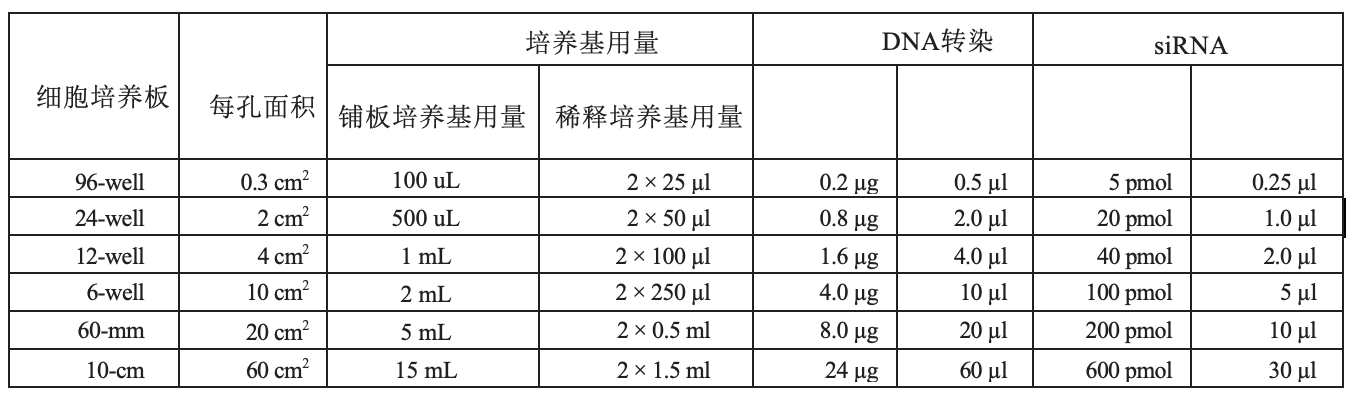
质粒DNA的转染 (每次转染一定要进行预实验,来摸索最佳条件, 尤其是转染试剂的最佳用量!)
对大多数细胞来说,DNA(µg)与Lipo2K (µl)的比例为1:2~1:3。转染时高的细胞密度可以得到高的转染效率和表达水平,并能减少细胞毒性。
贴壁细胞: 转染前一天,用500 µl不含抗生素的培养基接种0.5~2×105细胞,使之第二天能达到70-90%汇合。
悬浮细胞:在准备DNA-Lip2K复合物之前,用500 µl不含抗生素的培养基接种4~8×105细胞即可。
a. 在eppendorf管里分别加入50 µl Opti-MEM I ReLipced Serum Medium和0.8 µg DNA轻柔混匀,制成DNA稀释液。
c. 将DNA稀释液和Lipo2K稀释液混合,轻柔混匀,室温静置20分钟, 形成DNA-Lipo2K复合物。DNA-Lipo2K复合物在室温下可稳定存在6小时。
3. 将DNA-Lipo2K复合物加入到接种好的细胞中,将培养板轻轻地前后摇动,使复合物分散均匀。
4. 在37℃ CO2培养箱中培养4-6小时后更换培养基,继续培养18~48小时。
5. 如果要筛选稳定细胞株,则在转染24小时后将细胞按照1:10或更高的比例接种到新鲜培养基中,第二天加 入选择性培养基进行筛选。
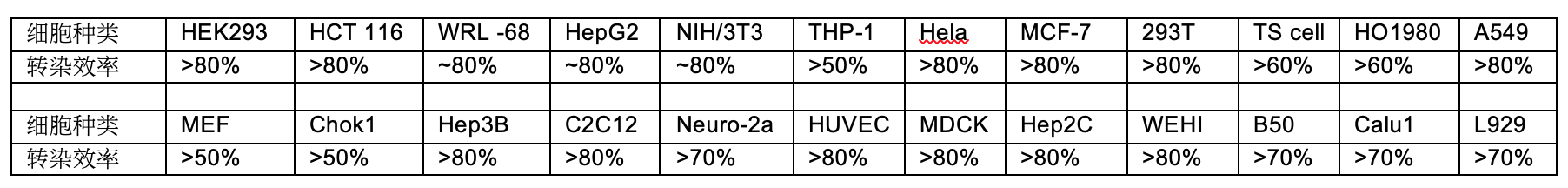
常见细胞的转染效率(富百科荧光显微镜自测数据,仅供参考,实验条件不同转染效率会有较大差别)
转染效率的测定方法: 1)实时定量PCR检测; 2)Western Blot检测; 3)流式细胞术 4)荧光显微镜: 转染含有荧光蛋白基因质粒DNA,通过荧光显微镜观察荧光的强弱以及荧光的效率。
细胞转染注意事项: 细胞/DNA/siRNA每次都不同,建议每次转染一定要进行预实验来摸索最佳条件,尤其是转染试剂的最佳用量!
2) 细胞的种类和状态影响较大:转染时细胞必须处于良好生长状态,转染时细胞的密度一般铺板率在达到70—80%最好(此时细胞处于对数生长期);
5) 转染时注意脂质体和用量,过量的话对细胞毒性大也容易失败。
8) 转染试剂对个别细胞可能有一定毒性,在转染过程由于提高细胞的通透性因而不能在培养答基中添加抗生素。
10) 培养基中的血清:在开始准备DNA和转染试剂稀释液时要使用无血清的培养基,因为血清会影响复合物的形成。其实,只要在DNA-转染试剂复合物形成时不含血清,在转染过程中是可以使用血清的。
11) 培养基中的抗生素:抗生素是影响转染的培养基添加物。这些抗生素一般对于真核细胞无毒,但阳离子脂质体试剂增加了细胞的通透性,使抗生素可以进入细胞。这降低了细胞的活性,导致转染效率降低。
12) 一般在转染24-48h,靶基因即在细胞内表达。根据不同的实验目的,24-48h后即可进行靶基因表达的检测实验。
13) 如若建立稳定的细胞系,则可对靶细胞进行筛选,根据不同基因载体中所含有的抗性标志选用相应的药物,常用的真核表达基因载体的标志物有潮霉素和新霉素等。
| Name | Lipo2K转染试剂 | ||
|---|---|---|---|
| CAT# | 029 | CAS# | N/A |
| Storage# | 4℃ Sealed&desiccated&Minimized light exposure | Shelf Life# | 18 months |
| Ex(nm)# | N/A | Em(nm)# | N/A |
| MW# | N/A | Solvent# | N/A |
| Name | Lipo2K转染试剂 |
|---|---|
| CAT# | 029 |
| CAS# | N/A |
| Storage# | 4℃ Sealed&desiccated&Minimized light exposure |
| Shelf Life# | 18 months |
| Ex(nm)# | N/A |
| Em(nm)# | N/A |
| MW# | N/A |
| Solvent# | N/A |

 详细说明书
详细说明书 技术资料
技术资料